Драгомира Николова
Драгомира Николова е молекулярен биолог със защитена докторантура в областта на онкогенетиката. Преподавател по „Медицинска генетика“ към Медицински университет – София. Специализирала е различни методи на генетичен анализ на човешкия геном в Лаборатория по молекулна медицина в Токио (Япония), както и биоинформатичен анализ в Лаборатория за анализ на геномни данни в институт Сан Рафаеле, Милано (Италия).
Затлъстяването е комплексно заболяване и се влияе от различни фактори като генетичния статус, поведението и околната среда. То се среща по-често в определени семейства – не толкова заради наследствеността, колкото заради еднаквия начин на хранене и общите лоши навици. Броят на хората със затлъстяване се повишава стабилно през последните 50 години и това не може да се обясни с драматични промени в нашите гени.
При съвместно изследване на Масачузетския технологичен институт и Харвардския медицински университет бе установен ген, чиято активация кара мастните клетки да горят енергията, складирана в тях. Такъв ефект е наблюдаван при лабораторни мишки, при които клетките – енергийни депа, са се превърнали в клетки, изгарящи енергия. Мазнините в човешкото тяло имат различна природа. Бялата мастна тъкан, която се натрупва основно в областта на корема, е основният „съхранител на енергия“. Кафявата мастна тъкан около врата и гръбначния стълб е свързана с изгаряне на енергия и производство на топлина. Учените отдавна се вълнуват от въпроса дали е възможно белите мастни клетки да се превърнат в кафяви? Този феномен би могъл да се постигне чрез генетично „превключване“. То се състои в активиране на генната експресия на гена FTO. Този ген е открит през 2007 година и показва категорична асоциация със затлъстяването. Около 44% от eвропейците носят вариант, който повишава риска за затлъстяване с около 30% или средно той носи около 3 кг телесно тегло в повече.
Предишни изследвания показват, че FTO се експресира в мозъка и повлиява апетита и чувството на глад, като влияе основно на мастните клетки. Предполага се, че FTO активира два други гена – IRX3 и IRX5, които насочват клетките към складиране на енергия. При слаби хора двата гена са изключени и в резултат на това клетките им изгарят енергия, вместо да я складират. Чрез съвременните техники за генно редактиране е възможно да се промени експресията на FTO в мастните клетки и те да се превръщат от складиращи в разграждащи мазнините, а мастната тъкан – от бяла, съответно, в кафява.
В хода на посоченото проучване били изследвани и мозъчните клетки при двете групи лица (с ниска и висока експресия на FTO) и разлика не била открита, което значи, че влиянието на гена се ограничава основно върху мастните, а не върху мозъчните клетки. От друга страна обаче, метаболизмът на собствените мастни клетки влияе повече върху теглото, отколкото диетата или физическите упражнения.
Лабораторни мишки с активен IRX3 ген имат средно с 15% по-високо тегло. След инактивиране на IRX3 и IRX5, мастните клетки постоянно изгарят енергия, независимо от количеството храна, която животните поемат или продължителността на съня им. От тези открития постепенно изкристализира идеята за създаване на лекарство, което да пуска/спира активността на IRX гените. Доколко обаче това лекарството ще бъде активно не се знае, защото превключването на гените става по време на ембрионалното развитие на мезенхимните тъкани и не е ясно дали това ще може да стане през живота на възрастния организъм.
Друга линия на изследователските търсения предполага, че ензимът TBK1 (TANK-binding kinase 1) e основен фактор, който регулира разхода на енергия в организма, респективно изгарянето на калории – както при отслабване, така и при напълняване. Този ген функционира по типа на обратната връзка и може да се сравни с

Тази пародия на „Марша на прогреса“ напомня, че в началото на века човечеството преминава една граница. За пръв път броят на хората с наднормено тегло превишава броя на хората с недостатъчно килограми
Par Salsero35 — File:Evolution-des-wissens.jpg, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=67395994
термостат, който реагира на промените в температурата и включва/изключва отоплението.
С помощта на миши модели се доказва, че хроничният стрес, предизвикан от наднорменото тегло, предизвиква възпаление чрез активацията на пътя на NFKB (важен път в клетките, регулиращ имунния отговор, растежа и клетъчната смърт). Този път активира поредица от гени, включително TBK1. Той, от своя страна, потиска AMPK – основен регулатор на разхода на енергия, като намалява способността на клетките да изгарят енергия и води до натрупване на мазнини. Така напълняването индуцира възпаление, което отново засилва пълнеенето. Обратно, когато TBK1 не е активен, AMPК засилва метаболизма на мастните клетки, в резултат на което те изгарят калории.
От друга страна, NKFB активира гена TBK1, а той, по типа на обратната връзка, може да инхибира NKFB. Активацията на TBK1 редуцира възпалението, макар да не го елиминира напълно. Но без TBK1, възпалението отново расте. Делецията (премахването) на TBK1 при затлъстели мишки води до загуба на тегло и повишаване на възпалението, но при мишки с нормално тегло не предизвиква никакви промени.
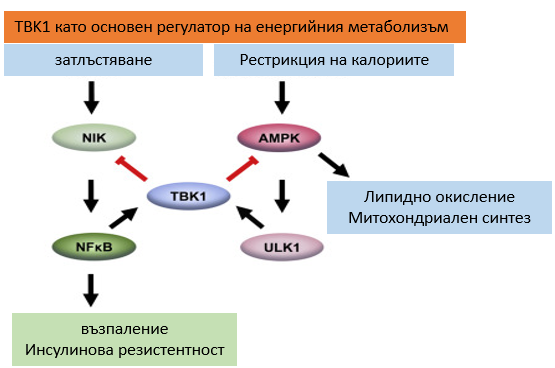
TBK1 на кръстопътя на възпалението и енергийната хомеостаза в адипозната (мастната) тъкан
Потискането на TBK1 има потенциал да възстановява енергийния баланс при състояние на затлъстяване, като повишава способността на клетките да изгарят мазнините. Днес се предполага, че това не е основният път за загуба на енергия, но все пак е насока за това как може да се въздейства върху метаболизма.
Един от възможните инхибитори на TBK1 се нарича амлексанокс (Amlexanox), противовъзпалително и противоалергично лекарство, използвано за лечение на астма, което е създадено през 1980 година в Япония.
Един от механизмите на неговото действие е да потиска възпалението, като намалява освобождаването на хистамин и левкотриени. Освен че потиска TBK1, има същия ефект и върху IKK-3 (Inflammatory Kinase) и така съдейства за намаляване на теглото и повишаване на чувствителността на клетките към инсулин. В статия, публикувана в сп. Cell Metabolism, се говори за значителна редукция на кръвната захар в клинично проучване на пациенти със захарен диабет, които са използвали амлексанокс за 12 седмици. Когато лекарството е давано на мишки със затлъстяване, те губели тегло, чувствителността им към инсулин се покачвала, повлиявайки положително върху диабета и стеатозата (омазняването на черния дроб).
Резултатите се подобряват при комбиниране на амлексанокс с тетрадецилтиооцетна киселина (TTA). Това е мастна киселина, която регулира отлагането на мазнини в клетките и контролира метаболизма. При прием помага на човек да се засити по-бързо и намалява чувството на глад. Освен това, тази мастна киселина има антивъзпалителни и засилващи имунитета свойства и не преминава процес на бета-окисление в митохондриите. Основни нейни ефекти са, че стимулира пролиферацията на митохондриите (увеличаване на броя на основни енергийни органели в клетката) в черния дроб и намалява серумните триглицериди (мазнини) и общия холестерол. В последните изследвания дори се твърди, че ТТА подобрява функцията на миокарда при сърдечна недостатъчност.
Основните ефекти на инхибитора амлексанокс са: 1. Намаляване на телесните мазнини, 2. Подобряване на глюкозния контрол, 3. Подобряване на инсулиновата резистентност, 4. Нормализиране на нивата на HbA1C (гликирания хемоглобин).
За съжаление, някои хора не се повлияват на лечението с амплексанокс. При тях той не действа и причината за това е все още неясна. Ето защо изследователите смятат, че все пак двупосочното действие остава най-печелившо: ограничаване на енергийния прием чрез диетата и повишаване на енергийния разход чрез изгаряне на повече калории. Само диетите не действат достатъчно ефективно.
Около 1% от световната популация са много слаби хора, независимо от това, че не спортуват или ядат много. Международен екип идентифицира кандидат-ген, отговорен за ниското тегло на някои хора. След анализиране на проби от 47 000 човека от Естонската биобанка бил установен генът ALK, който потиска натрупването на мазнини при метаболитно слаби хора. При отстраняване(делеция) на ALK при лабораторни мишки, те, мишките остават слаби и това доказва, че този ген регулира разхода на енергия. Лекарства инхибитори на ALK се използват сравнително отдавна при лечение на някои видове рак. Дали прилагането на ALK инхибиторите е свързано с дълготрайно намаляване на теглото предстои да бъде установено в бъдеще.
Изследвания на ALK гена при Drosophila (плодова мушица) и мишки показват, че потискането на генната експресия води до резистентност към натрупване на тегло при висококалорийна диета. За разлика от FTO, ALK има висока експресия и в мозъка и директно „инструктира“ мастните клетки да активират мастния си метаболизъм. Естонската национална биобанка е много подходяща за такова изследване, защото включва хора от широк възрастов диапазон (между 18 и 44 години) с ясни фенотипни характеристики. По-нататъшните изследвания следва
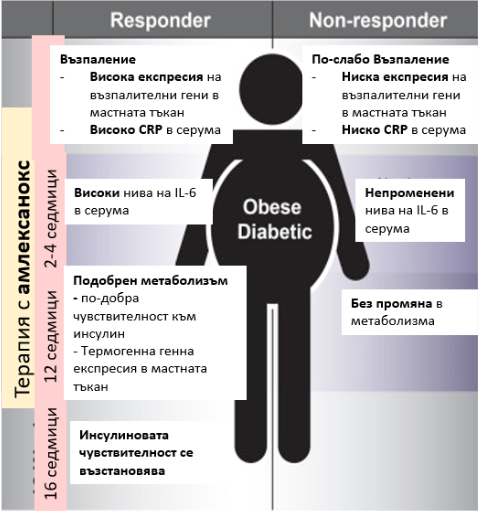
Повлияващи се (responders) и неповлияващи се (non-responders) пациенти на терапията с амлексанокс
да репликират (повторят) резултатите при друга голяма група пациенти и последващи метаанализи. Ако резултатите при хората се сравнят с мишки и плодови мушици, ще се установи еволюционното дърво на метаболизма, ролята на ALK и подлежащите биохимични и генетични зависимости.
ALK генът, обаче, не е единствената причина хората да бъдат постоянно слаби. Независимо, че ролята му вече е доказана, все пак съществуват и други фактори, които действат в комбинация с „добрите гени“:
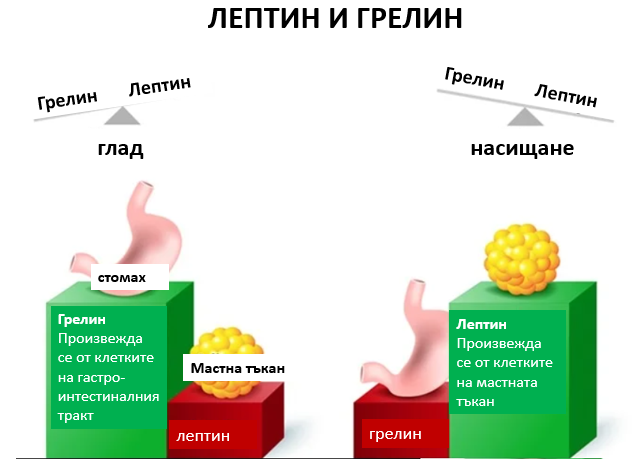
Действие на лептина и грелина
– Те имат навика да ядат само когато са наистина гладни. Понякога става въпрос за психическо пристрастяване към храната, а при тях то отсъства.
– Гладът се контролира от два хормона – грелин и лептин. Лептинът, който се продуцира от мастните клетки, потиска апетита, докато грелинът има обратно действие – той стимулира апетита. Хората с повишена чувствителност към лептин или повишена продукция на този хормон могат по-лесно да контролират теглото си.
Грелинът е хормон, произведен от ентероендокринните клетки на гастроинтестиналния тракт, особено в стомаха и често се нарича „хормон на глада“. Нивата му са най-високи при усещане за глад и се нормализират след хранене. Този хормон подготвя тялото за прием на храна – стимулира движението на червата и секрецията на стомашен сок.Релинът въздейства пряко върху мозъка, като активира клетките на хипофизната жлеза и хипоталамуса, включително невропептид У невроните, които отговарят за апетита.
От своя страна лептинът е хормон, основно синтезиран от мастните клетки и ентероцитите в тънкото черво. Той спомага за поддържане на баланса като потиска глада и намалява отлагането на мазнини в мастните клетки. Той действа върху клетъчни рецептори в хипоталамуса в мозъка, като ги насища. При затлъстяване се развива понижена чувствителност на клетките към лептин (подобно на инсулиновата резистентност при тип 2 диабет). Така пълните хора не получават чувство на ситост, независимо от повишеното отлагане на енергия и високите нива на лептин.
Отдавна е известно, че сънят също има отношение към теглото. Хормоните се регулират най-добре при поне 7 часа сън на денонощие. Липсата на сън води до постоянно високи нива на грелин, а тялото свръхпродуцира кортизол – хормон, който събужда глада. Накратко, повече сън води до по-ниско тегло. Добрите хранителни навици също имат значение. Ако ядем бавно и дъвчем повече, мозъкът има по-дълго време да сигнализира тялото, че е настъпило засищане.
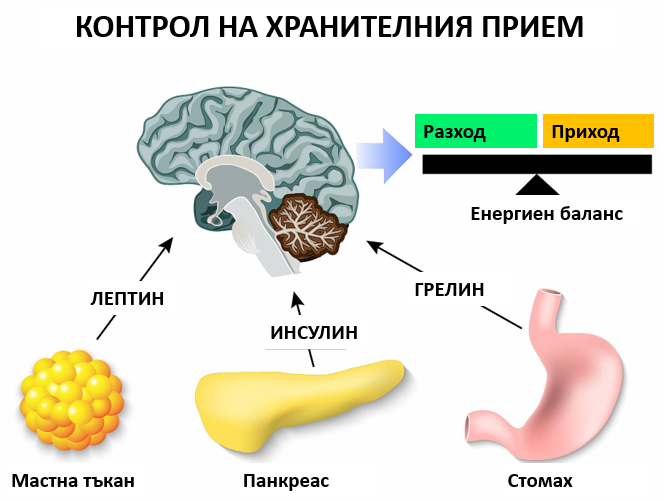
Хормонален контрол на хранителния прием
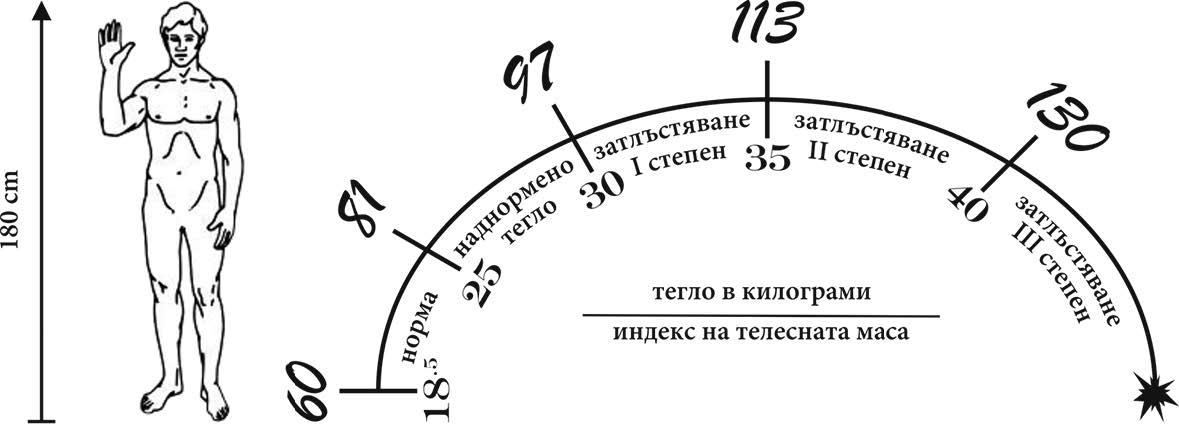
Нормално тегло (кг) и степени на затлъстяване при ръст 180 cm
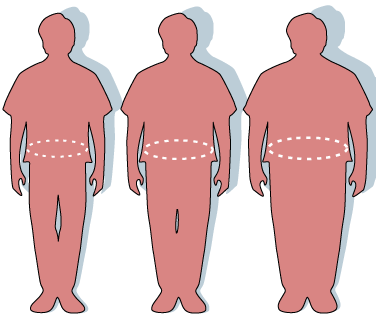
Силуети и обиколки на талията, които показват нормално телосложение (вляво), наднормено тегло (в средата) и затлъстяване (вдясно). Схема Уикипедия
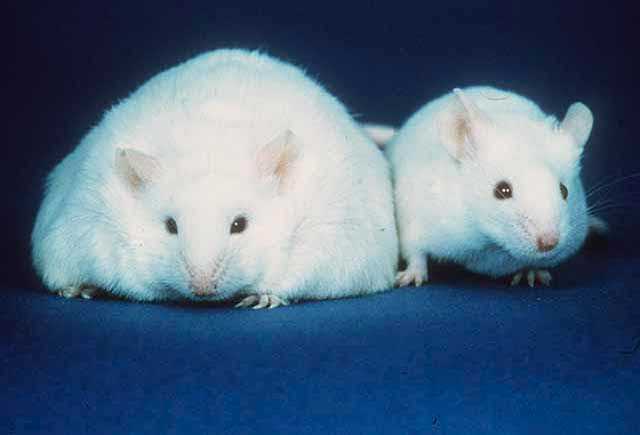
Сравнение между мишка, неспособна да произвежда лептин, което води до затлъстяване (вляво) и нормална мишка (вдясно)
И затлъстяването, и патологичната слабост днес се считат не само за козметичен дефект. Те са комплексни заболявания, мултифакторни, социалнозначими и до голяма степен предотвратими. И докато за слабостта няма все още ясни данни, то затлъстяването и наднорменото тегло засягат 30% от световната популация днес. Според някои прогнози до 2030 година, около 38% от световната популация в зряла възраст ще е с наднормено тегло, а 20% – със затлъстяване. Първенството по отношение на тази тенденция все още се държи от САЩ, но все повече от развиващите се страни почти достигат тези нива. Това показва необходимостта
и нуждата от нови, ефективни лекарствени средства за контрол и баланс на енергийния метаболизъм. Неслучайно натискът върху фармацевтичната индустрия все повече нараства, а наличните продукти все още са ненапълно ефективни и безопасни.
Публикуван сп. Природа бр 3/2021 г. стр. 80 – 85